
Perzierjet homogjene dhe heterogjene
Substancat në natyrë ndodhen në gjendje të pastër ose në trajtë përzierjesh.
- Të pastra janë për shembull
,
,
,
,
etj.
- Përzierje janë për shembull
,
,
etj.
Përzierjet janë bashkësi substancash. Substancat e pastra dhe përzierjet ndodhen në të tria gjendjet fizike: të ngurtë, të lëngët dhe të gaztë. Ndryshimi midis substancave të pastra dhe përzierjeve shpjegohet me faktin se substanca e pastër është një dhe e vetme.

Eksperiment: Marrim dy gota kimike dhe në secilën prej tyre hedhim nga 100g . në gotën e parë shtojmë 10g sulfat bakri kristalhidrat(
). Në gotën e dytë hedhim 10g rërë. Më anën e një thupre qelqi përziejmë përbërësit në gota. Shohim se në gotën e parë, kristalet e sulfatit treten dhe ngjyra e kaltër shpërndahet në mënyrë të njëtrajtshme në të gjithë masën e ujit. Formohet përzierje homogjene.
Përbërësit e përzierjes homogjene nuk mund të dallohen të veçuar nga njëri-tjetri.
Ndërsa, në gotën e dytë, megjithëse e përziejmë herë pas here, rëra grumbullohet në fund të gotës. Ajo nuk tretet dhe mund të veçohet në çdo moment nga uji. Kjo përzierje quhet heterogjene.
Përbërësit e përzierjes heterogjene mund të shihen me sy të lirë.
Nga ky eksperiment, nxjerrim se përzierjet ndahen në dy grupe:
- Homogjene,
- Heterogjene
Përzierja homogjene e përbërë nga dy ose më shumë substanca quhet tretësirë.
Përbërësit e tretësirës përzihen në raporte në masë, që lëvizinn në kufij të gjerë. Ata nuk dallohen me sy të lirë, as me mikroskop.
Pjesët përbërëse të tretësirës janë: tretësi dhe substanca e tretur.
- Tretësi është substanca që ndodhet në sasi më të madhe në tretësirë. Ai është një i vetëm dhe ka po atë gjendje fizike si dhe tretësira. Tretësirat më të përdorshëm janë: uji, alkooli, benzina, por, si tretës mund të jetë edhe një substancë e ngurtë ose e gaztë.
- Substanca e tretur ndodhet në sasi më të vogël në tretësirë. Ajo mund të jetë e ngurtë, e lëngët ose e gaztë. Në një tretësirë mund të ketë më shumë se një substancë të tretur.
Tretësirat mund të jenë në gjendje të ngurtë, të lëngët ose të gaztë.
Në eksperimentin më sipër, në gotën e parë, sulfati i bakrit është substance e tretur, ndërsa uji është tretësi.
Tretshmëria e substancave në ujë
Uji, veçoritë e tij
Formula molekularee e ujit është .
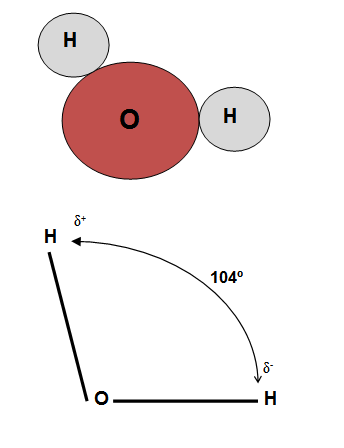
Në skemën më sipër, vihet re se atomet e hidrogjenit kanë fituar ngarkesë të pjesëshme (+), ndërsa atomi i oksigjenit ngarkesë të pjesëshme (-), për shkak të zhvendosjes së çifteve elektronike të përbashkëta në drejtim të atomit të oksigjenit. Kjo zhvendosje ndodh sepse oksigjeni është element elektronegativ, ndërsa hidrogjeni është element elektropozitiv.
Nga kjo del se në molekulën e formohen dy pole:
- Poli pozitiv nga ana e atomeve të hidrogjenit,
- Poli negative nga ana e atomit te oksigjenit.
Themi se molekulat e ujit kanë karakter polar dhe uji është një tretës polar.
Eksperiment 1: Në tri gota qqë përmbajnë 100 gramë secila, hedhim përkatësisht: në të parën 10 gramë klorur natriumi, në të dytën 10 gramë karbonat kalciumi. Vëmë re se në gotën e parë
tretet plotësisht, në gotën e dytë
tretet pjesërisht, ndërsa në gotën e tretë
nuk tretet..
Nga eksperimentet ka dalë se një pjesë e substancave treten mirë në ujë, një pjesë e tyre treten pak në ujë dhe disa substanca të tjera nuk treten në ujë.
Substanca plotësisht të patretshme nuk ka.
Përkufizim: “Tretshmëria është aftësia që ka një substancë për t’u tretur në një tretës të dhënë”.
Në kuptimin sasior, ajo shpreh sasinë në gramë të substancës së tretur në 100 gramë tretës, në një temperaturë të caktuar.
Eksperiment 2: Hedhim pak sheqer në një gotë me ujë dhe përmbajtjen e gotës e përziejmë. Sheqeri tretet. Në tretësirën e përftuar shtojmë pak nga pak sasi të tjera sheqeri duke e përzier vazhdimisht dhe tretësira vazhdon të tresë sheqer.
Tretësira, që ka aftësi të tresë akoma sasi substancë të tretur, quhet e pangopur.
Duke hedhur akoma sheqer, vjen një çast kur substanca e ngurtë ngelet e patretur në fund të gotës. Në këtë rast tretësira quhet e ngopur.
Kur tretësira përmbanë një sasi të vogël substance të tretur në një sasi të dhënë tretësi, quhet tretësirë e holluar.
Kur ajo përmbanë sasi të mëdha substance të tretur në të njëjtën sasi të dhënë të tretësit, quhet tretësirë e përqëndruar.
Faktorët që ndikojnë në tretjen e substancave në një tretës të dhënë
Pamë që substancat ndahen në tre grupe:
- Të tretshme
- Pak të tretshme
- Të patretshme
Mund të themi që çdo substancë ka aftësi të caktuar për t’u tretur në një tretës të dhënë, aftësi kjo që është e lidhur me disa faktorë të cilët ndikojnë në proçesin e tretjes. Këta faktorë janë:
- Natyra kimike e tretësit dhe e substancës së tretur
Në tretësit polarë treten mirë përbërjet me lidhje jonike ose kovalente polare.
Në tretësit jopolarë treten mirë përbërjet me lidhje kovalente jopolare.
- Shkalla e grimcimit të substancës së tretur
Sheqeri pluhur tretet më mirë se sheqeri kristalor. Kjo shpjegohet me rritjen e sipërfaqes së kontaktit midis molekulave të sheqerit dhe molekulave të ujit.
- Ndikimi i temperaturës
Kur treten substanca të ngurta në ujë, përgjithësisht tretshmëria është në përpjestim të drejt me ndryshimet e temperaturës.
- Trysnia ndikon vetëm tek gazet
Tretshmëria e gazeve në ujë është në përpjestim të zhdrejtë me temperaturën, porn ë përpjestim të drejt me trysninë.

